위 이미지를 클릭하시면 인터넷으로 바로 문제를 풀어 보실수 있습니다.
(해설, 모의고사, 오답노트, 워드, 컴활, 정보처리 상설검정 프로그램 기능 포함)
전자문제집 CBT란?
종이 문제집이 아닌 인터넷으로 문제를 풀고 자동으로 채점하며 모의고사, 오답 노트, 해설까지 제공하는
무료 기출문제 학습 프로그램으로 실제 상설검정에서 사용하는 OMR 형식의 CBT를 제공합니다.
최신 화학분석기사 필기 기출문제(해설) : [다운로드]
화학분석기사 필기 기출문제(해설) 및 전자문제집 CBT 2021년09월12일| 1. | 할로겐 원소의 특성을 설명한 것 중 틀린 것은? |
| 4. | 수소와 반응하여 할로겐화수소를 생성한다. |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 86%
| | <문제 해설>
주기가 커질수록 반응성이 감소한다!
F>Cl>...
[해설작성자 : 김수야니] |
|
| 2. | 유효숫자 계산이 정확한 것만 고른 것은? |
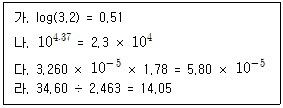
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 61%
| | <문제 해설>
곱셈의 경우 유효숫자의 갯수가 낮은 쪽으로 맞춤 |
|
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 71%
| | <문제 해설>
C1H4 : 1
C2H6 : 1
C3H8 : 1
C4H10 : 2
C5H12 : 3
C6H14 : 5
C7H16 : 9
[해설작성자 : 바다아이] |
|
| 4. | 분석방법에 대한 검증은 인증 표준물질(CRM)과 표준물질(RM) 또는 표준용액을 사용하여 검증한다. 다음 중 분석방법에 대한 검증항목이 아닌 것은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 77%
| | <문제 해설>
시험법 밸리데이션의 주요 항목
정확성
정밀성 - 반복정밀성
정밀성 - 실간정밀성
정밀성 - 실내정밀성
특이성
검출한계
정량한계
직선성
범위
완건성
기타 용액안정성 및 검체안정성, 시스템적합성 항목을 볼 수 있으나, 안전성에 대한 평가는 분석법 밸리대이션 항목이 아님.
[해설작성자 : 티케이맥스] |
|
| 5. | 단색화 장치의 성능을 결정하는 요소로서 가장 거리가 먼 것은? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 57%
| | <문제 해설>
단색화장치(Monochromator)는 흔히들 사용하는 UV spectrophotometer에서 특정 파장대의 광원을 선택하는 장치.
광원이 되는 복사선의 순도, 특정파장만을 선택할 수 있는 근접파장 분해능력, 띠 너비에 따른 분해능차이 와 같은 parameter가 있다
[해설작성자 : 티케이맥스] |
|
| 6. | 자외선-가시광선 분광기의 구성 요소가 아닌 것은? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 79%
| | <문제 해설>
지시전극은 전위차측정기에서 검체를 측정하는데 사용하는 전극
[해설작성자 : 티케이맥스] |
|
| 7. | 폴리스타이렌(polystyrene)에 대한 설명으로 틀린 것은? (단, 폴리스타이렌 단량체의 분자량은 104 g/mol 이다.) |
| 1. | 스타이렌이 1000개 연결되어 생성된 폴리스타이렌은 1.04×105 g/mol 의 분자량을 가진다. |
| 2. | 폴리스타이렌의 단량체는 페닐기를 포함한다. |
| 3. | 대표적인 열경화성 수지 가운데 하나이다. |
| 4. | 폴리스타이렌 생성 반응은 개시(intiation), 생장(propagation), 종결(termination)의 세단계로 이루어진다. |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 74%
| | <문제 해설>
폴리스타이렌은 대표적인 열가소성 수지 입니다!
[해설작성자 : 김수야니] |
|
| 8. | H2(g) + I2(g) → 2HI(g) 반응의 평형상수(Kc)는 430℃에서 54.3 이다. 이 온도에서 1L 용기 안에 들어있는 각 화학종의 몰수를 측정하니 H2는 0.2mol, I2는 0.15mol 이라면, HI의 농도(M)는? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 57%
| | <문제 해설>
54.3=x^2/(0.2*0.15)
x=1.2763...=1.28
[해설작성자 : 여리] |
|

정답 : [3]☜ 블럭 설정하면 보임
정답률 : 71%
| | <문제 해설>
모체가 되는 탄화수소 사슬을 정한다.
모체가 되는 작용기를 특정한다.
모체 에서 나온 가지 사슬을 특정한다.
작용기나 가지 사슬이 2개 이상 있는 경우 우선 순위가 가장 높은 작용기 또는 가지 사슬이 가장 낮은 번호가 되어야 한다.
[해설작성자 : 티케이맥스] |
|
| 10. | 일정한 온도와 압력에서 진행되는 아래의 연소반응에 관련된 내용 중 틀린 것은? |
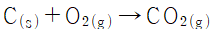 | 1. | 0.5mol의 탄소가 0.5mol의 산소와 반응하여 0.5mol의 이산화탄소를 만든다. |
| 2. | 1g의 탄소가 1g의 산소와 반응하여 1g의 이산화탄소를 만든다. |
| 3. | 이 반응에서 소비된 산소가 1mol이었다면, 생성된 이산화탄소의 몰수는 1mol이다. |
| 4. | 이 반응에서 1L의 산소가 소비되었다면, 생성된 이산화탄소의 부피는 1L 이다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 90%
| | <문제 해설>
1mol의 탄소가 1mol의 산소와 반응하여 1mol의 이산화탄소를 만든다.
[해설작성자 : 김수야니]
12g의 탄소가 32g의 산소와 반응하여 44g의 이산화탄소를 만든다.
[해설작성자 : 조금일하고많이벌자] |
|
| 12. | 원자와 관련된 용어에 대한 설명 중 틀린 것은? |
| 1. | 이온화 에너지는 양이온 생성 시 원자가 흡수하는 에너지이다. |
| 2. | 전기 음성도는 결합 시 원자가 전자를 끌어당기는 정도를 나타내는 값이다. |
| 3. | 원자가 전자란 원자의 최외각에 배치하여 화학결합에 관여하는 전자이다. |
| 4. | 전자 친화도는 음이온 생성 시 원자가 흡수하는 에너지이다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 60%
| | <문제 해설>
전자 친화도는 음이온 생성 시 방출하는 에너지를 말합니다^^
[해설작성자 : KangCorn] |
|
| 3. | 273K, 1atm에서 이상기체인 He 0.224L |
| 4. | 이산화탄소 분자 0.01몰 내에 들어있는 총 산소 원자 |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 79%
| | <문제 해설>
1. 산소 1mol =18g 0.01mol = 0.18g
2. 탄소 1mol =14g 0.01mol = 0.14g
3. 헬륨 1mol =2g PV=nRT n=PV/RT=1*0.224/0.0821*273=0.00999mol 0.00999mol*2g/mol=0.02g
4. 이산화산소 1mol속 산소 질량 =32g 0.01mol = 0.32g
[해설작성자 : 김수야니]
아래와 같은 오류 신고가 있었습니다.
여러분들의 많은 의견 부탁 드립니다.
추후 여러분들의 의견을 반영하여 정답을 수정하도록 하겠습니다.
참고로 정답 변경은 오류 신고 5회 이상일 경우 수정합니다.
[오류 신고 내용]
산소 1mol 16g 탄소 1mol 12g 입니다
[해설작성자 : 바다아이]
[추가 오류 신고]
산소원자 1mol = 16g, 따라서 산소원자 0.01mol = 0.016g
질소원자 1mol = 14g, 따라서 질소원자 0.01mol = 0.014g
헬륨 1mol = 4g, 따라서 STP 상태의 헬륨 0.224L = 0.1mol = 0.4g
이산화 탄소 1mol = 44g, 이산화탄소 1mol속 산소의 질량은 32g, 따라서 이산화탄소 0.01mol속 총 산소의 무게는 0.32g
따라서 답은 3번
[해설작성자 : 꽃깝돌]
[오류신고 반론]
보기의 헬륨은 0.01몰이 맞습니다. 정답은 3번이 아닌 4번 입니다.
[해설작성자 : 박건욱] |
|
| 14. | 다음 중 원자의 크기가 가장 작은 것은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 87%
| | <문제 해설>
같은 족 원소끼리는 원소번호가 커질수록 원자의 크기도 커짐
[해설작성자 : 화분기 뿌셔] |
|
| 15. | 11.99g의 염산이 녹아있는 5.48M 염산 용액의 부피(mL)는? (단, Cl의 원자량은 35.45 g/mol 이다.) |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 78%
| | <문제 해설>
M=mol/L
HCl(M) = 11.99/36.45=0.329mol
0.329mol/5.48M = 0.060L
1L=1000ml
0.60*1000=60
[해설작성자 : or늑한나무]
원자량 35.45로 계산하면 정답 61 나와요
[해설작성자 : 화분기 내일 시험…]
위 해설답변분이 미리 경고해주신건지 모르겠는데
HCl은 36.45
Cl만 계산해야 35.45 나와용
[해설작성자 : 화분기 내일모레 시험] |
|
| 16. | 11.3g의 암모니아 속에 들어있는 수소원자의 몰수(mol)는? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 77%
| | <문제 해설>
M=mol/L
NH3(M) = 11.3/17=0.665mol
0.665*3=1.995
약2.0
[해설작성자 : 김수야니] |
|
| 17. | 적외선 분광법의 시료용기 재료로 가장 부적합한 것은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 63%
| | <문제 해설>
적외선 분광법에서 사용하는 시료용기는 이온성 물질을 사용해야 합니다.
[해설작성자 : KangCorn] |
|
| 18. | 두 개의 탄화수소기가 산소원자에 결합된 형태를 가진 분자이며, 두 개의 알코올 분자로부터 한 분자의 물이 탈수되어 생성되는 분자의 종류는? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 73%
| | <문제 해설>
ROH + R'OH > ROR' + H2O
ROH, R'OH: 알콜(alcohol)
ROR': 에터(ether)
[해설작성자 : 조금일하고많이벌자] |
|
| 19. | 국가표준기본법령상 제품등이 국가표준, 국제표준 등을 충족하는지를 평가하는 교정, 인증, 시험, 검사 등을 의미하는 용어는? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 64%
|
| 20. | 주기율표상에서 나트륨(Na)부터 염소(Cl)에 이르는 3주기 원소들의 경향성을 옳게 설명한 것은? |
| 1. | Na로부터 Cl로 갈수록 전자 친화력은 약해진다. |
| 2. | Na로부터 Cl로 갈수록 1차 이온화 에너지는 커진다. |
| 3. | Na로부터 Cl로 갈수록 원자반경은 커진다. |
| 4. | Na로부터 Cl로 갈수록 금속성이 증가한다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 81%
| | <문제 해설>
금속성: 전자를 잃고 양이온이 되려는 성질
원자반경: 원자궤도는 같은데 원자핵의 전하량이 커져서 오히려 감소한다.
1차 이온화 에너지: 엄밀하게 말하면 증가 약간 감소 증가~~~ 약간 감소 증가~ 라서 틀린 표현이 맞다.
가장 맞게 설명한 것은 이온화 에너지라 이온화 에너지를 정답으로 한 걸로 보임.
전자친화력: =전기 음성도 족이 증가할수록 주기가 감소할수록 커짐.
[해설작성자 : Rivolo] |
|
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 87%
| | <문제 해설>
1. 5
2. 4
3. 2
4. -3
[해설작성자 : 김수야니] |
|
| 22. | Pb2+와 EDTA의 형성 상수(formation constant)가 1.0×1018이고 pH 10에서 EDTA 중 Y4-의 분율이 0.3일 때, pH 10에서 조건(conditional) 형성 상수는? (단, 육양성자 형태의 EDTA를 H6Y2+로 표현할 때, Y4-는 EDTA에서 수소가 완전히 해리된 상태이다.) |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 58%
| | <문제 해설>
형성상수 = 조건형성상수 x edta 몰분율
1.0x10^18 = 조건형성상수 X 0.3
[해설작성자 : 오늘싰ㆍ]
아래와 같은 오류 신고가 있었습니다.
여러분들의 많은 의견 부탁 드립니다.
추후 여러분들의 의견을 반영하여 정답을 수정하도록 하겠습니다.
참고로 정답 변경은 오류 신고 5회 이상일 경우 수정합니다.
[오류 신고 내용]
조건형성상수 = 형성상수 * edta 분율
[해설작성자 : ㅎ]
[오류신고 반론]
조건형성 상수= 형성상수 * Y4-분율
[해설작성자 : 다들 힘내] |
|
| 23. | 다음 중 Hg2(IO3)2(s)를 용해시킬 때, 용해된 Hg22+의 농도가 가장 큰 것은? (단, Hg2(IO3)2(s)의 용해도곱상수는 1.3×10-18 이다.) |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 69%
| | <문제 해설>
간단하게 물에 이온이 많으면 다른 이온을 감싸면서 마치 그 이온이 없는 것과 같은 현상이 나타남.
없는 걸로 간주되니깐 용해도가 증가하는 현상이 발생.
[해설작성자 : Rivolo] |
|
| 24. | 산과 염기에 대한 설명 중 틀린 것은? |
| 1. | 산은 물에서 수소이온(H+)의 농도를 증가시키는 물질이다. |
| 2. | 산과 염기가 반응하여 물과 염을 생성하는 반응을 중화반응이라고 한다. |
| 3. | 염기성 용액에서는 H+ 의 농도보다 OH-의 농도가 더 크다. |
| 4. | 산성용액은 붉은 리트머스 시험지를 푸르게 변색시킨다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 89%
| | <문제 해설>
산성용액은 푸른 리트머스 시험지를 붉게 변색시킨다.
[해설작성자 : 김수야니] |
|
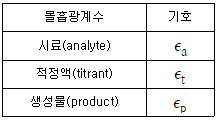
| 25. | 활동도 계수의 특성에 대한 설명으로 가장 거리가 먼 것은? |
| 1. | 농도가 높지 않은 용액에서 주어진 화학종의 활동도 계수는 전해질의 종류에 따라서만 달라진다. |
| 2. | 용액이 무한히 묽어짐에 따라 주어진 화학종의 활동도 계수는 1로 수렴한다. |
| 3. | 주어진 이온세기에서 같은 전하를 가진 이온들의 활동도 계수는 거의 같다. |
| 4. | 전하를 띠지 않은 분자의 활동도 계수는 이온세기에 관계없이 대략 1 이다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 62%
| | <문제 해설>
활동도 계수는 농도와 온도에 민감하기 때문에 농도가 높지 않은 용액이어도 달라진다.
[해설작성자 : 만거] |
|
| 26. | 0.1000M HCl 용액 25.00mL에 0.1000M NaOH 용액 25.10mL를 가했을 때의 pH는? (단, Kw는 10-14 이다.) |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 64%
| | <문제 해설>
[H+] 몰수 = 0.1000M * 25.00mL = 2.500mmol
[OH-] 몰수 = 0.1000M * 25.10mL = 2.510mmol
[OH-]의 몰수가 [H+]의 몰수보다 많으므로 반응 후 [OH-]가 남는다.
반응 후 [OH-] = (2.510-2.500)mmol/(25.00+25.10)mL = 1.996*10^-4M
pOH = -log[OH-] = 3.700
pH = 14-pOH = 10.30
[해설작성자 : 조금일하고많이벌자] |
|
| 27. | 0℃에서 액체 물의 밀도는 0.9998 g/mL 이고 이온화상수는 1.14×10-15 이다. 0℃에서 액체 물의 해리 백분율(mol%)은? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 36%
| | <문제 해설>
H2O ↔ H+ + OH-
(-x) (+x) (+x)
-----------------------
a-x x x
x^2 = 1.14x10^-15
x = 3.376 x 10^-8 M = [H+] = [OH-]
*H2O 가 1 ml 있다고 가정하면
0.9998g
H+의 몰수 = 3.376x10^-8 M * 1ml = 3.376x10^-8 mmol
H2O의 초기 몰수 = 0.9998g/18g/mol = 0.0555mol = 55.5mmol
평형 상태의 몰수= 55.5mmol - 3.376x10^-8mmol (훨씬 작은 수이므로 무시할 수 있음)
= 55.5mmol
해리 백분율 = (3.376x10^-8 / 55.5) x 100 = 6.1x10^-8
[해설작성자 : KangCorn] |
|
| 28. | UV/Vis 흡수 분광법에 관한 설명 중 틀린 것은? |
| 1. | 유기화합물의 UV-Vis 흡수는 n 또는 π 궤도에 있는 전자가 π*궤도로 전이하는 것에 기초로 두고 있다. |
| 2. | n → π*전이에 해당하는 몰흡광계수는 비교적 작은 값을 갖는다. |
| 3. | π → π*전이에 해당하는 몰흡광계수는 대부분 큰 값을 갖는다. |
| 4. | 용매의 극성이 증가하면 n → π*전이에 해당하는 흡수 봉우리는 장파장 쪽으로 이동한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 71%
| | <문제 해설>
UV-Vis 흡수 분광법에서 n → π* 보다 π → π* 의 효율이 더 좋음.
따라서 몰흡광계수도 더 큰 값을 가짐
용매의 극성이 증가하면 에너지가 증가함
에너지와 파장은 역비례하므로
에너지가 증가할수록 파장은 짧아지고 단파장 쪽으로 이동하쥬
[해설작성자 : KangCorn] |
|
| 29. | X선 분광법에서 파장을 분리하는 단색화 장치에 이용되는 분신요소는? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 46%
| | <문제 해설>
X선분광법에서 단색화 장치는 빛살 평행화장치와 분산요소로 구성되며, 빛살 평행화장치는 금속판, 분산요소는 결정이다.
[해설작성자 : 만거 ] |
|
| 30. | 이온 세기와 이와 관련된 현상에 대한 설명 중 틀린 것은? |
| 1. | 이온세기는 용액 중에 있는 이온의 전체 농도를 나타내는 척도이다. |
| 2. | 염을 첨가하면, 이온 분위기가 형성되어 더 많은 고체가 녹는다. |
| 3. | 염을 증가시키면 이온 간 인력이 순수한 물에서 보다 감소한다. |
| 4. | 이온 세기가 클수록 이온 분위기의 전하는 작아진다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 58%
| | <문제 해설>
이온 세기가 클수록 이온 분위기의 전하도 커집니다 쑥쑥
[해설작성자 : KangCorn] |
|
| 31. | 약산 용액을 강염기 용액으로 적정할 때 적절한 지시약과 적정이 끝난 후 용액의 색이 올바르게 연결된 것은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 74%
| | <문제 해설>
페놀프탈레인 지식약
산성 : 무색
중성 : 무색
염기 : 빨강
[해설작성자 : 김수야니]
메틸레드,메틸오렌지: 산성지시약
붉은색(산성)-노란색(염기성)
페놀레드,페놀프탈레인:염기성지시약
페놀레드 노란색(중성)- 붉은색(염기성)
페놀프탈레인 무색(중성)-붉은색(염기성)
[해설작성자 : 과락하는중] |
|
| 32. | 다음의 전기화학 전지에 대한 설명으로 틀린 것은? |
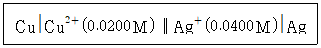 | 1. | 한줄 수직선(Ⅰ)은 전위가 발생하는 상 경계나 전위가 발생할 수 있는 접촉면이다. |
| 2. | 이중 수직선(Ⅱ)은 염다리의 양 끝에 있는 두 개의 상 경계이다. |
| 3. | 0.0400M은 은이온(Ag+)의 농도이다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 81%
| | <문제 해설>
Cu의 반응성이 Ag보다 크므로, Cu는 산화전극
[해설작성자 : 조금일하고많이벌자] |
|
| 33. | 0.050M 염화트리메틸암모늄((CH3)3NH+Cl) 용액의 pH는? (단, 염화트리메틸암모늄의 Ka는 1.59×10-10 이고, Kw는 1.0×10-14 이다.) |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 51%
| | <문제 해설>
pH = -log ( 루트(Ka*c) )
= -log (1.59x10^-10 * 0.05)^1/2 = 5.549… = 5.55
[해설작성자 : KangCorn]
위 풀이는 해리 상수가 매우 작은 경우에만 적용 가능합니다. ( 거의 해리 안되는 경우에만 c가 0.05 그대로니깐 )
정확한 식은
x^2 / (0.05-x) = 1.59*10^(-10)
x = 2.82*10^(-6)
-log(x) = 5.549
solve 기능 사용하시면 편합니다.
[해설작성자 : Rivlo] |
|
| 34. | 황산구리(Ⅱ) 수용액으로부터 구리를 석출하기 위해 2A의 전류를 흘려주려고 한다. 1.36g의 구리를 석출하기 위해 필요한 시간(s)은? (단, 1F는 96500 C/mol이며, 구리의 원자량은 63.5 g/mol 이다.) |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 54%
| | <문제 해설>
1.36(g) / 63.5(g/mol) * (96500C/mol * 0.5) ( 황산 제2구리라 2당량 이므로 2로 나눠줘야함) * 2 = 2066
[해설작성자 : ㅇㅇㅇㅇ] |
|
| 35. | 원자 분광법에서 이온의 형성을 억제하기 위한 방법으로 적절한 것은? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 56%
| | <문제 해설>
온도를 올리면 원자끼리 붙어있기 더워서 이온화가 잘 일어나며
압력을 올리면 공간이 좁아져서 이온화가 일어나지 않고 붙어있다 생각하면 편해용
[해설작성자 : 김수야니] |
|
| 36. | Ag 및 Cd와 관련된 반쪽 반응식과 표준 환원 전위가 아래와 같을 때, 25℃에서 다음 전지의 전위(V)는? |

정답 : [4]☜ 블럭 설정하면 보임
정답률 : 62%
| | <문제 해설>
Nernst Equation
E = E0 - 0.0592/n * logQ
Ag^+의 E0 더 크므로 환원 전위
Cd^2+의 E0 더 작으므로 산화 전위
산화 전위 식을 반대로 돌리자!
2Ag^+ + Cd → 2Ag + Cd^2+
[Cd^+2]
Q = -------
[Ag^+]^2
E = (0.799+0.402) - 0.0592/2 * log (0.1)/(0.5)^2
= 1.2127…
= 1.213
[해설작성자 : KangCorn] |
|
| 4. | 녹이 슬면서 일정 시간 질량이 감소하다가 일정하게 된다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 80%
| | <문제 해설>
철은 공기중에 산소와 만나서 녹스는 것이기 때문에 질량은 증가!
[해설작성자 : 김수야니] |
|
| 38. | 온도가 증가할 때, 아래 두 반응의 평형상수 변화는? |
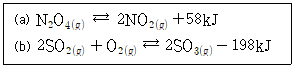
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 61%
| | <문제 해설>
외부 T 가 증가하면 평형 T는 감소하는 방향으로 진행된다.
(a)는 발열 반응이므로 온도를 감소시키려면 역반응이 진행되어야 하며 평형 상수가 감소함
(b)는 흡열 반응이므로 온도를 감소시키려면 정반응이 진행되어야 하며 평형 상수가 증가함
[해설작성자 : KangCorn] |
|
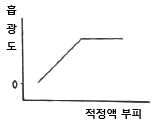
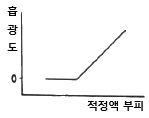
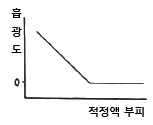
| 39. | 산-염기 적정에서 사용하는 지시약의 반응과 지시약의 형태에 따른 색상이 아래와 같다. 중성인 용액에 지시약과 산을 첨가하였을 때 혼합용액의 색깔은? |
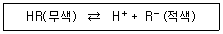
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 74%
| | <문제 해설>
중성 : 무색
염기성 : 적색(빨강)
을 띠는 지시약은 페놀프탈레인으로
산성일 때는 무색을 띤다.
페놀프탈레인 : 무무빨
[해설작성자 : 김수야니] |
|
| 40. | 높은 몰흡광계수를 갖는 시료를 분석할 때, 다음 중 Beer's law가 가장 잘 적용될 수 있는 경우는? |
| 1. | 분석물의 농도범위가 10-4 ~ 10-3M 일 때 |
| 2. | 분석물의 농도범위가 10-3 ~ 10-2M 일 때 |
| 3. | 분석물의 농도범위가 10-2 ~ 10-1M 일 때 |
| 4. | 분석물의 농도범위가 10-1 ~ 100M 일 때 |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 62%
| | <문제 해설>
Beer's Law는 농도가 묽은 용액에서 잘 적용됨
[해설작성자 : comcbt.com 이용자]
A=ebc 에서 A는 같은 값이니까 e가 증가하면 c(농도)는 작아야 함
[해설작성자 : 22년 1회차 화이팅] |
|
| 41. | 온도 변화에 따른 시료의 무게 감량을 측정하는 분석법은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 83%
| | <문제 해설>
FT-IR 적외선 분광법
TGA : 질량 변화 측정
GPC : 용매의 크기를 기준으로 분류하는 크로마토 그래피
GC/MS : 가스 크로마토그래피 - 질량 분석
+
DTA 온도 변화 측정
DSC 에너지 변화 측정
[해설작성자 : KangCorn] |
|
| 42. | 전압-전류법의 전압-전류 곡선으로부터 얻을 수 있는 정보가 아닌 것은? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 56%
|
| 43. | 원자 질량 분석법(Atomic Mass Spectrometry)의 이온화 방법으로 틀린 것은? |
| 2. | 글로우 방전(glow discharge) |
| 3. | 장 이온화 방출침(field inoization emitter) |
| 4. | 유도 결합 플라스마(inductively coupled plasma) |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 46%
| | <문제 해설>
장 이온화 방출법은 분자 질량 분석법
[해설작성자 : KangCorn] |
|
| 44. | Gas Chromatography(GC)에서 사용되는 검출기와 선택적인 화합물의 연결이 잘못된 것은? |
| 2. | NPD – 질소(N), 인(P) 포함 화합물 |
| 4. | TCD – 운반 기체와 열전도도 차이가 있는 화합물 |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 72%
| | <문제 해설>
FID는 유기화합물
[해설작성자 : KangCorn] |
|
| 45. | 핵 자기 공명(Nuclear Magnetic Resonance, NMR) 분광법에서 사용 가능한 내부 표준물로 가장 적절한 것은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 67%
| | <문제 해설>
NMR에서 사용하는 내부 표준물은 TMS, DSS 두개만 생각하면 됩니다
(CH3)4Si = TMS
[해설작성자 : KangCorn] |
|
| 46. | 열무게 분석법(TGA)의 주된 응용(연구)으로 거리가 먼 것은? |
| 4. | 기화, 승화, 탈착과 같은 물리적 변화 연구 |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 56%
| | <문제 해설>
중합체 분해반응의 속도론적 연구는 DSC
[해설작성자 : KangCorn] |
|
| 47. | 핵 자기 공명(Nuclear Magnetic Resonance, NMR) 분광법에 대한 설명으로 틀린 것은? |
| 2. | 화학종의 구조를 밝히는데 주로 사용된다. |
| 3. | 흡수과정에서 원자의 핵이 관여하지 않는다. |
| 4. | 4~900 MHz 정도의 라디오 주파수 영역의 전자기 복사선의 흡수를 측정한다. |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 79%
| | <문제 해설>
원자의 핵과 자기장의 관계로 분자 구조를 밝힌다.
[해설작성자 : 만거] |
|
| 48. | 전해질(0.1M KNO3)만 있는 용액에서 적하 수은 전극(D.M.E.)에 –0.8V를 적용하고 측정한 잔류 전류(residual current)는 0.2μA 이다. 같은 전해질 용액 100mL에 포함된 Cd2+ 환원에 대한 한계 전류(liniting current)는 8.0μA 이다. 만약 1.00×10-2M Cd2+ 표준용액 5mL를 이 용액에 가한 후 –0.8V에서 측정한 한계 전류가 11.0μA라면, 이 용액에 포함된 Cd2+의 농도(mM)는? (단, 측정 간 온도변화는 없다고 가정한다.) |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 24%
| | <문제 해설>
첫 번째에서 확산전류는 8.0 - 0.2 = 7.8uA이다. 두 번째 확산 전류는 11.0 - 0.2 = 10.8uA이다.
Cd2+의 농도를 c라고 하고 확산 전류와 농도 관련 식을 쓰면, 100c + 5 x 10 / 105c = 10.8 / 7.8이다. 따라서 [Cd2+] = 1.10mM
[해설작성자 : 신쫄이 레콜맛]
아래와 같은 오류 신고가 있었습니다.
여러분들의 많은 의견 부탁 드립니다.
추후 여러분들의 의견을 반영하여 정답을 수정하도록 하겠습니다.
참고로 정답 변경은 오류 신고 5회 이상일 경우 수정합니다.
[오류 신고 내용]
5x10이 아니라 5x10^-2 아닌가요,,?
[해설작성자 : 아니라면 죄송합미닷]
[오류신고 반론]
5*10이 맞습니다
주어진 단위는 5*10^-2M이고
해설 작성자님께서는 계산하기 편하게 5*10mM로 바꿔서 넣으신 겁니다.
[해설작성자 : Rivolo]
[오류신고 반론]
문제 해설 보충합니다. 위에 풀이는 너무 많이 생략했습니다.
원래 확산-한계전류 I = k*c 입니다. 바꿔 말해, I1:I2 = kc1:kc2 (상수k는 같은 물질이므로 제거 )
I1c2 = I2c1 -> I2/I1 = c2/c1 입니다. 농도 c = 몰 수*부피 입니다.
보기 불편하니깐 '('는 제발 씁시다.
정확한 풀이는 ( c = 농도 )
(( 100ml * c + 5*10 mmol ) / 105 ml ) / c = 10.8/7.8 입니다
제 생각이랑 공식이 계속 달라서 왜 다른가 했네요
[해설작성자 : Rivolo] |
|
| 1. | 전기량의 단위로 F(Faraday)가 사용되는데 1F는 96485 C/mole e-로 되는데 1C는 1V×1A 이다. |
| 2. | 전기량법 적정은 전해전지를 구성한 분석용액에 뷰렛으로부터 표준용액을 가하면서 전류의 변화를 읽어서 종말점을 구한다. |
| 3. | 조절-전위 전기량법을 위한 전지는 기준전극(reference electrode), 상대전극(counter electrode), 및 작업전극(working electrode)으로 구성되는데 기준전극과 상대전극 사이의 전위를 조정한다. |
| 4. | 구리의 전기분해 전지에서 전위를 일정하게 놓고 전기분해를 하면 시간에 따라 전류가 감소하는데 이는 구리 이온의 농도가 감소하고 환원전극 농도 편극의 증가가 일어나기 때문이다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 49%
| | <문제 해설>
1. 1C = 1A * 1s
2. 전기량법은 전류를 일정하게 유지합니다 이후 종말점까지 소요된 전기량을 측정하는 거쥬
3. 상대 전극과 작업 전극 사이의 전위입니다
4. 소거법으로 정답.
e- -> ┌─│l│l ─┐
불순물+Cu │ │ Cu
~~~~~~~~~~~~~~~~~~~
Cu2+
Cu에서 2e- 가 나오면서 이온화, 2e-를 받고 Cu2+가 석출 반복하면
Cu 이온의 농도는 변하지 않음.
다만 불순물이 이온화하여 불순물 이온이 생기고, 여기서 나온 전자를 받아 Cu 이온이 석출되면
구리 이온의 농도는 줄어들게 되는데 이 내용을 가정으로 해야 4번이 맞음
[해설작성자 : KangCorn] |
|
| 50. | 적외선 흡수 스펙트럼을 나타낼 때 가로축으로 주로 파수(cm-1)를 쓰고 있다. 파장(μm)과의 관계는? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 75%
| | <문제 해설>
1cm = 10mm = 10^4μm
단위만 맞춰도 바로 답이 나오네요.
[해설작성자 : 조금일하고많이벌자] |
|
| 51. | FT-IR에서 789cm-1와 791cm-1의 흡수 밴드를 구별하기 위해 거울이 움직여야 하는 거리(cm)는?(문제 오류로 가답안 발표시 1번으로 발표되었지만 확정답안 발표시 모두 정답처리 되었습니다. 여기서는 가답안인 1번을 누르면 정답 처리 됩니다.) |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 77%
| | <문제 해설>
R = 1/2l
(l = 흡수 밴드 간 거리)
= 1/2*(791-789)cm^-1
= 1/2*2cm^-1 = 0.25cm (보기에 정답 없음)
[해설작성자 : Always August] |
|
| 52. | 분자 질량 분석법의 이온화 방법 중 사용하기 편리하고 이온 전류를 발생시키므로 매우 예민한 방법이지만, 열적으로 불안정하고 분자량이 큰 바이오 물질들의 이온화원에는 부적당한 방법은? |
| 1. | Electron Ionization(EI) |
| 2. | Electro Spray Ionization(ESI) |
| 3. | Fast Atom Bombardment(FAB) |
| 4. | Matrix-Assisted Laser Desorption Ionization(MALDI) |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 63%
| | <문제 해설>
EI 는 사용하기 편리해 많이 쓰이고 특히 기체에 가장 잘 적용됨 하지만 온도가 높아 분자를 쉽게 쪼개버림(토막내버림)
그래서 분자량이 큰 바이오 물질을 적용 시키면 분자량이 쪼개져서 제대로 된 측정을 할 수 없음
[해설작성자 : KangCorn]
온도를 올려 시료를 기화 -> 전자빔 충돌
시료의 기화가 필수이므로
이온화 전 열분해 가능성이 있음
[해설작성자 : Always August] |
|
| 53. | HPLC에서 역상(reversed-phase) 크로마토그래피 시스템을 가장 잘 설명한 것은? |
| 1. | 정지상이 극성이고 이동상이 비극성인 시스템 |
| 2. | 이동상이 극성이고 정지상이 비극성인 시스템 |
| 3. | 분석 물질이 극성이고 정지상이 비극성인 시스템 |
| 4. | 정지상이 극성이고 분석 물질이 비극성인 시스템 |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 76%
| | <문제 해설>
HPLC 정상 크로마토그래피 : 정지상 - 극성, 이동상 - 비극성
HPLC 역상 크로마토그래피 : 이동상 - 극성, 정지상 - 비극성
[해설작성자 : 김수야니]
+정상에서 정지상으로 물을 쓸 수 있어 편리하다는 점을 기억하면
정지상 - 극성, 이동상은 반대인 - 무극성
[해설작성자 : KangCorn] |
|
| 54. | Gas Chromatography(GC)의 이상적인 검출기의 특징으로 틀린 것은? |
| 3. | 검출기의 감도는 10-8 ~ 10-15g 용질/s 일 때 이상적이다. |
| 4. | 흐름 속도와 무관하게 긴 응답 시간을 가져야 한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 85%
| | <문제 해설>
응답 시간은 빠를 수록 좋습니다
[해설작성자 : KangCorn] |
|
| 55. | 시료와 기준 물질의 온도를 프로그램 하여 변화시킬 때, 두 물질 간의 온도차(△T)를 측정하여 분석하는 열분석법은? |
| 1. | Thermal Gravimetric Analysis(TGA) |
| 2. | Differential Thermal Analysis(DTA) |
| 3. | Differential Scanning Calorimetry(DSC) |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 73%
| | <문제 해설>
TGA → 질량의 변화
DTA → 온도의 변화
DSC → 에너지의 변화
[해설작성자 : KangCorn] |
|
| 56. | 질량 분석법으로 얻을 수 있는 정보가 아닌 것은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 63%
| | <문제 해설>
질량 분석법은 이온을 만들어서 강한 자기장에 통과시켜 휘게 만듬
무거운 녀석들은 가까운 곳에 떨어질 것이고 가벼운 녀석들은 멀리 갈 것임
이러한 측정 방법에서 전자는 관여하지 않기 때문에 반응성에 대한 정보는 얻을 수 없음
[해설작성자 : KangCorn] |
|
| 57. | 컬럼의 길이가 30cm인 크로마토그래피를 사용하여 혼합물 시료로부터 성분 A를 분리하였다. 분리된 성분 A의 머무름 시간은 12분이었으며, 분리된 봉우리 밑변의 너비가 2.4분이었다면 이 컬럼의 단높이(cm)는? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 53%
| | <문제 해설>
H=L/N
=30/16{(12/2.4)^2}
=0.075
[해설작성자 : 아이고] |
|
| 58. | 시차 주사 열계량법(Differential Scanning Calorimetry; DSC)에 대한 설명으로 틀린 것은? |
| 1. | 시료 물질과 기준 물질을 조절된 온도 프로그램에서 가열하면서 두 물질의 온도 차이를 온도의 함수로서 측정한다. |
| 2. | 전력보상 DSC와 열흐름 DSC에서 제공하는 정보는 같으나 기기장치는 근본적으로 다르다. |
| 3. | 폴리에틸렌의 DSC 자료에서 발열 피크의 면적은 결정화 정도를 측정하는데 이용된다. |
| 4. | DSC 단독 사용 시 물질종의 확인은 어려우나, 물질의 순도는 확인할 수 있다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 55%
| | <문제 해설>
두 물질의 온도 차이를 "시간"의 함수로서 측정한다.
[해설작성자 : 김수야니]
제가 문제 해설 써놓고 제가 틀렸네요,,, 헤헤
시료 물질과 기준 물질을 조절된 온도 프로그램에서 가열하면서 두 물질의 "에너지(OR열유속) 차이"를 온도의 함수로서 측정한다.
참고로 1번은 DTA에 대한 설명 입니다!!!!!!!!!!!!
[해설작성자 : 김수야니] |
|
| 59. | ICP-MS의 작동 순서와 설명으로 틀린 것은? |
| 1. | ICP를 켜기 전 냉각수 및 진공 상태를 확인한다. |
| 2. | 플라스마를 켠 다음, 플라스마 작동조건을 최적화 시킨다. |
| 3. | 시료 도입 전에 바탕 용액으로 잠깐 동안 시료 도입 장치의 조건을 맞춘다. |
| 4. | 실험이 끝나면 플라스마를 끄고, 약산으로 시료 도입 장치를 세척한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 71%
| | <문제 해설>
약산은 유기산이 많으므로 세척 후 남아 있는 물질이 존재해 씻는 의미가 없음
세척 시 강산을 사용해야 함
[해설작성자 : KangCorn] |
|
| 60. | 유리 지시 전극을 사용하여 용액의 pH를 측정할 때에 대한 설명으로 가장 적절하지 않은 것은? |
| 3. | 높은 pH에서는 알칼리 오차가 생길 수 있다. |
| 4. | 내부 용액의 수소 이온농도를 정확히 알고 있어야 한다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 46%
| | <문제 해설>
선택계수는 1보더 작아야 한다.
[해설작성자 : 화분기 화이팅 ] |
|
| 61. | 원료의약품의 정량 시험을 밸리데이션하는 과정에서 얻은 결과 중 틀린 것은? (단, 허용기준은 R≥0.990이다.) |
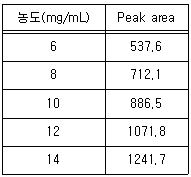
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 68%
| | <문제 해설>
Y절편 : + 5.99
[해설작성자 : 만거] |
|
| 62. | 검량선 작성에 관한 내용 중 틀린 것을 모두 고른 것은? |

정답 : [2]☜ 블럭 설정하면 보임
정답률 : 42%
|
| 1. | 동일 실험실내에서 동일한 시험자가 동일한 장치와 기구, 동일제조번호와 시약, 기타 동일 조작 조건하에서 균일한 검체로부터 얻은 복수의 검체를 짧은 기간차로 반복분석 실험하여 얻은 측정값들 사이의 근접성을 검토해야 한다. |
| 2. | 동일한 실험실내에서 다른 실험일, 다른 시험자, 다른 기구 또는 장비 등을 이용하여 분석 실험하여 얻은 측정값들 사이의 근접성을 검토해야 한다. |
| 3. | 일반적으로 표준화된 시험방법을 사용하여 서로 다른 실험실에서 하나의 동일한 검체로부터 얻은 측정값들 사이의 근접성을 검토해야 한다. |
| 4. | 분석대상물질의 양에 비례하여 일정 범위 내에 직선적인 측정값을 얻어낼 수 있는 능력을 검토해야 한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 50%
| | <문제 해설>
4번은 직선성에 대한 설명
[해설작성자 : KangCorn] |
|
| 64. | 광화학반응용기 및 전기영동법의 모세관 칼럼의 재질로 가장 많이 사용되는 물질은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 76%
| | <문제 해설>
SiO2 실리카를 제일 많이 쓰는데
이게 바로 석영
[해설작성자 : KangCorn] |
|
| 65. | 시험법 밸리데이션 계획서의 구성이 아래와 같을 때, 계획서에 대한 설명 중 틀린 것은? |
 | 1. | 시험에 사용되는 장비, 물질, 시험조건 등을 상세히 기술한다. |
| 2. | 시험법 밸리데이션의 항목은 시험의 목적에 맞게 선택할 수 있다. |
| 3. | 허용범위는 시험 결과에 따라 달라질 수 있다. |
| 4. | 시험 용액의 제조 등과 같이 시험법과 관련된 내역을 상세히 기술한다. |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 75%
| | <문제 해설>
허용 범위가 달라지면 재시험 해야 합니다
[해설작성자 : KangCorn] |
|
| 66. | Volumetric Karl Fischer를 사용하여 실험한 결과가 아래와 같을 때, 실험 결과의 해석 및 일반적인 장비관리절차를 기준으로 적절하지 않은 의견을 제시한 사람은? |
 | 1. | 이대리 : %RSD가 이상있으니 전극의 상태를 먼저 점검해볼 필요가 있어 보입니다. |
| 2. | 류과장 : 그럼 교체주기와 사용이력 등을 먼저 확인해 보도록 합시다. |
| 3. | 김부장 : 장비에 문제가 발생하였다고 보여지면 외부의 업체에 의뢰하여 Calibration을 실시하는 것도 좋겠어요. |
| 4. | 권사원 : 외부에 의뢰할 예정이니 장비 유지보수 기록서는 별도로 기입하지 않겠습니다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 81%
| | <문제 해설>
권사원은 시말서를 제출해야 할 것입니다...
칼피셔는 민감한 기기이므로 유지 보수 기록 중요합니다...
그리고 실제로 칼피셔는 저렇게 말을 안 듣습니다... 저도 모르고 싶었습니다...
[해설작성자 : 김수야니] |
|
| 67. | 아래 측정값의 평균(A), 표준편차(B), 분산(C), 변동계수(D), 범위(E)는? |
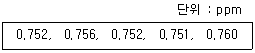 | 1. | A : 0.754, B : 0.004, C : 1.4×10-5, D : 0.5%, E : 0.009 |
| 2. | A : 0.754, B : 0.003, C : 1.4×10-5, D : 0.1%, E : 0.09 |
| 3. | A : 0.754, B : 0.004, C : 1.4×10-6, D : 0.5%, E : 0.09 |
| 4. | A : 0.754, B : 0.003, C : 1.4×10-6, D : 0.1%, E : 0.009 |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 61%
|
| 68. | 평균값이 ±4% 이내일 때, 95%의 신뢰도를 얻기 위한 2.8g 시료의 분석 횟수는? (단, 분석 불정확도는 시료 채취 불정확도보다 매우 작아 무시할 만하며, 주어진 조건에서 시료채취상수는 41g 이다.) |
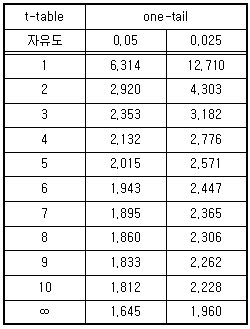
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 48%
| | <문제 해설>
t(자유도) * s (상대표준편차) (%)
신뢰구간 = 평균값 x̅ ± -------------------------------
√n 실험 횟수
시료채취상수 공식
mR2 = Ks (시료채취상수)
2.8g * R2= 41g
R = 3.82… (%)
t * 3.82
±4% = -----------
√n
신뢰도는 0.05 = 90%, 0.025 = 95%
자유도는 n-1 값을 이용한다.
ex) n=5 , 4번 테이블의 값인 2.776 대입
t * 3.82
----------- < n=6, t= 2.571 값을 대입했을 때 값이 4가 나오므로 n=6 >
√n
[해설작성자 : KangCorn] |
|
| 69. | 시험분석기관의 부서를 사업 총괄부서와 시험장비 운용부서로 나눌 때, 사업총괄부서의 시험장비 밸리데이션 관련 임무와 거리가 먼 것은? |
| 3. | 소관기관 시험장비에 대한 밸리데이션 사업 시행에 필요한 예산을 확보한다. |
| 4. | 표준수행절차 및 표준 서식 등을 정하고 필요·요구에 맞게 수정·보완한다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 64%
| | <문제 해설>
2번은 시험장비 운용부서의 임무
[해설작성자 : 만거] |
|
| 70. | 다음은 검출 한계를 특정하는 여러 방법 중 한 가지이다. ( )에 들어갈 내용을 바르게 연결된 것은? |

정답 : [1]☜ 블럭 설정하면 보임
정답률 : 53%
|
| 71. | Na+을 포함하는 미지시료를 AES를 이용해 측정한 결과 4.00mV이고, 미지시료 95.0mL에 2.00M NaCl 표준용액 5.00mL를 첨가한 후 측정하였더니, 8.00mV였을 때, 미지시료 중에 함유된 Na+의 농도(M)는? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 46%
| | <문제 해설>
미지시료 95ml → 4.00mV
미지시료 95ml + 2.00M NaCl 5ml → 8.00mV
농도가 바뀜에 따라 전압이 바뀌는 것을 인지.
비례식으로 풀 수 있다.
미지시료에도 Na+가 존재할 것임.
2.00M * 5.00ml = 10mmol
x mmol x+10 mmol
4.00mV : -------- = 8.00mV : ----------
95ml 100ml
식을 풀면 x = 9.05mmol
문제는 미지시료에 존재하는 Na+의 농도를 물었으므로
9.05 mmol
M = ------------ = 0.095 M
95 ml
[해설작성자 : KangCorn] |
|
| 72. | 분석의 전처리 과정에서 발생 가능한 오차에 대한 설명 중 적합하지 않은 것은? |
| 1. | 측정에서 오차는 측정 조건에 따라 그 크기가 달라지지만 아무리 노력하더라도 오차를 완전히 없앨 수 없다. |
| 2. | 우연 오차는 동일한 시험을 연속적으로 실시하여 보정이 가능하다. |
| 3. | 우연 오차에서는 평균값보다 큰 측정값이 얻어질 확률과 작은 값이 얻어질 확률이 같다. |
| 4. | 계통 오차의 발생 예는 교정되지 않은 뷰렛을 사용하여 부피를 측정하였을 때를 들 수 있다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 65%
| | <문제 해설>
우연 오차는 외부 요소에 의한 것이므로 실험을 반복한다고 해결할 수 있는 것이 아님
[해설작성자 : KangCorn] |
|
| 73. | 분석을 시작하기 전 매트릭스가 혼재되어 있을 때 보조적인 시험방법을 추가로 고려해야 하는지의 여부를 결정짓는 특성은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 54%
| | <문제 해설>
완건성 : 시험방법 개발 단계에서 고려하는 평가항목,
조건이 의도적으로 변경되었을 때 측정값이 영향을 받는 지에 대한 척도
견뢰성 : 정상적인 시험 조건의 변화 하에서 동일한 시료를 분석한 실험 결과의 재현성 정도,
시험법이 시험 변수에 영향을 받는 정도
[해설작성자 : KangCorn]
특이성은 불순물, 분해물, 배합성분 등의 혼재 상태에서 분석대상물질을 선택적으로 정확하게 측정할 수 있는 능력이다.
[해설작성자 : 만거] |
|
| 74. | 분석장비를 이용한 실험 준비 과정에 대한 설명 중 옳은 것을 모두 고른 것은? |

정답 : [2]☜ 블럭 설정하면 보임
정답률 : 82%
| | <문제 해설>
디젤 차량도 워밍업을 하는데..
보통 이온화 시킬 때, 기체화 시킬 때 등 온도를 높혀서 분석하는 경우가 많음.
워밍업 시간이 필요합니다.
[해설작성자 : KangCorn] |
|
| 75. | 시험법 밸리데이션 과정에 일반적으로 요구되는 방법 검증 항목을 모두 고른 것은?(오류 신고가 접수된 문제입니다. 반드시 정답과 해설을 확인하시기 바랍니다.) |

정답 : [1]☜ 블럭 설정하면 보임
정답률 : 59%
| | <문제 해설>
아래와 같은 오류 신고가 있었습니다.
여러분들의 많은 의견 부탁 드립니다.
추후 여러분들의 의견을 반영하여 정답을 수정하도록 하겠습니다.
참고로 정답 변경은 오류 신고 5회 이상일 경우 수정합니다.
[오류 신고 내용]
제가 알기로는..
시험법 밸리데이션에 안정성은 포함되지 않는 걸로 알고 있습니다.
검증항목: 검출한계, 정량한계, 선택성, 정밀성(반복성, 실험실내/실험실간), 정확성, 범위, 직선성, 완건성(?) 으로 알고 있습니다. 정답 확인 부탁드립니다.
[해설작성자 : Rivolo]
[오류신고 반론]
안전성은 포함되지 않고, 안정성은 포함
[해설작성자 : 호랑이] |
|
| 76. | 시험법 밸리데이션 항목 중 직선성 평가에 대한 설명으로 옳지 않은 것은? |
| 1. | 적어도 5개 농도의 검체를 사용하는 것이 권장된다. |
| 2. | 최소자승법에 의한 회귀 직선의 계산과 같은 통계학적 방법을 이용해 측정 결과를 평가한다. |
| 3. | 농도 또는 함량에 대한 함수로 그래프를 작성하여 시각적으로 직선성을 평가한다. |
| 4. | 만약 시험결과가 허용범위에 만족하지 못하는 경우 해당 시험법은 밸리데이션 될 수 없다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 51%
| | <문제 해설>
4. 관계가 직선적이지 않다면 비직선형의 원인을 밝혀내거나 시험방법에서 직선성을 나타내는 범위로 측정을 제한한다.
[해설작성자 : 만거] |
|
| 77. | 시험, 교정 또는 샘플링 성적서에 관한 KS의 일부분이 아래와 같을 때, 밑줄 친 것에 해당하지 않는 것은? |

정답 : [1]☜ 블럭 설정하면 보임
정답률 : 59%
| | <문제 해설>
누가, 무엇을 의뢰 했는지 중요하지 날짜는 중요하지 않다.
[해설작성자 : KangCorn] |
|
| 78. | GC-MS를 이용한 VOCs 실험에서 밸리데이션 실험 요소에 따른 평가기준 설정으로 적절하지 않은 것은? (단, 공정시험법을 기준으로 한다.) |
| 1. | 정량한계 근처의 농도가 되도록 분석물질을 첨가한 시료 7개를 준비하여 각 시료를 공정시험법 분석절차와 동일하게 추출하여 표준편차를 구한 후 표준편차의 3.14를 곱한 값을 방법검출한계로, 10을 곱한 값을 정량한계로 나타낸다. |
| 2. | 검정곡선의 작성 및 검증은 정량범위 내의 3개 이상의 농도에 대해 검정곡선을 작성하고, 얻어진 검정곡선의 결정계수(R2)가 0.98 이상이어야 한다. |
| 3. | 검정곡선의 작성 및 검증은 정량범위 내의 3개 이상의 농도에 대해 검정곡선을 작성하고, 얻어진 검정곡선의 상대표준편차가 25% 이내이어야 한다. |
| 4. | 정확도 기준은 정제수에 정량한계 농도의 2배~10배가 되도록 표준물질을 첨가한 시료를 3개 이상 준비하여 공정시험법 분석절차와 동일하게 측정한 측정 평균값의 상대 백분율이 50%~150% 이내이어야 한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 53%
| | <문제 해설>
4. 정량한계 농도의 "10배"가 되도록 표준물질을 첨가한 시료를 "4개" 이상 준비하여
[해설작성자 : KangCorn] |
|
| 79. | 시험법 밸리데이션에 관한 설명 중 일반적인 수행방법으로 가장 거리가 먼 것은? |
| 1. | 시험법 밸리데이션의 목적은 시험방법이 목적에 적합함을 증명하는 것이다. |
| 2. | 밸리데이션을 수행할 때는 순도가 명시된 특성 분석이 완료된 표준물질을 사용해야 한다. |
| 3. | 밸리데이션 시에 확보한 모든 관련 자료와 항목에 적용한 산출공식을 제출하고 적절하게 설명해야 한다. |
| 4. | 밸리데이션된 시험방법의 변경사항에 대한 기록은 생략 가능하다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 83%
|
| 80. | 분석 시료의 균질성을 확보하기 위한 방법으로 가장 거리가 먼 것은? |
| 1. | 정제(알약)의 경우 무게와 크기가 표준품 규격에 일치하는 1정을 선별하여 분석시료를 제조한다. |
| 2. | 액제(물약)의 경우 시료 채취 전 충분히 교반 후 상·중·하층으로 나누어 채취 후 혼합하여 분석 시료를 제조한다. |
| 3. | 휘발성 물질의 경우 채취 중 외부와의 접촉을 최소화하며 분석 시료 보관 용기를 가득 채운다. |
| 4. | 지하수의 경우 물을 충분히 퍼낸 다음 새로 나온 물을 채취한다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 55%
| | <문제 해설>
한 번만 하는 실험은 없다.
정밀성을 확보하기 위해 여러 번 실험을 진행해야 함
규격에 일치하는 "20정"을 선별하여
[해설작성자 : KangCorn] |
|
| 81. | 아연과 황산을 반응시키는 아래의 반응으로 생성되는 수소를 수상포집한다. 반응 종료 후 포집병 내부의 부피는 125mL, 전체압력은 838torr, 온도는 60℃일 때, 수소의 몰분율과 반응에 소모된 아연의 양(g)은? (단, 포집병 내부에는 수증기와 수소만 있다고 가정하며, 60℃의 수증기압은 150torr이고, 아연의 원자량은 65.37 g/mol 이다.) |
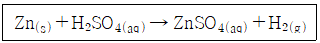
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 39%
| | <문제 해설>
포집병 안에는 수증기와 수소가 존재한다.
따라서 전체 압력 = P_H2 + 150torr
PV=nRT
부피와 온도가 일정하므로 P=n 압력과 몰수가 비례함을 알 수 있다.
수소의 몰 분율 X_H2 = (838-150)/838 = 0.82
위 반응식을 살펴보면,
반응에 소모된 아연의 몰 수와 생성된 수소의 몰 수는 1:1로 동일하다.
n_H2 = n_Zn
(838-150)torr *1atm/760torr * 0.125L = n_H2 * 0.0821 atm*L/mol*K * 333 K
위 식을 정리하면
n_H2 = n_Zn = (838-150) * 0.125 / (760*0.0821*333)
Zn의 몰 수 = 0.00414mol
아연의 양 (g) = 0.00414mol * 65.37g/mol = 0.270g
[해설작성자 : KangCorn] |
|
| 82. | 과학기술정보통신부의 연구실 설치·운영 가이드라인상 산화제와 같이 보관해서는 안되는 화학물질은? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 55%
| | <문제 해설>
산화제는 유기물과 폭발적 반응을 하므로 같이 보관해서는 안된다.
[해설작성자 : 김덕배] |
|
| 83. | 폐기물관리법령상 폐기물분석전문기관이 아닌 것은? (단, 그 밖에 환경부장관이 폐기물 시험·분석 능력이 있다고 인정하는 기관은 제외한다.) |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 59%
|
| 84. | 실험실에서의 시약 사용 시 주의사항, 폐기물 처리 및 보관 수칙 중 틀린 것은? |
| 1. | 시약은 필요한 만큼만 시약병에서 덜어내어 사용하고, 남은 시약은 재사용하지 않고 폐기한다. |
| 2. | 폐시약을 수집할 때는 성분별로 구분하여 보관 용기에 보관하며, 남은 폐시약은 물로 씻고 하수구에 폐기한다. |
| 3. | 폐시약 보관 용기는 통풍이 잘 되는 곳을 별도로 지정하여 보관한다. |
| 4. | 폐시약 보관 용기는 저장량을 주기적으로 확인하고 폐수 처리장에 처리한다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 82%
| | <문제 해설>
폐시약이 물과 반응하는 것일 수 있으므로 물로 씻으면 안됩니다.
하수구가 아닌 폐기통에 모아서 처리해야 합니다.
[해설작성자 : KangCorn] |
|
| 85. | 완전연소할 때 자극성이 강하고 유독한 기체를 발생하는 물질은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 77%
| | <문제 해설>
이황화탄소 완전연소 반응식 : CS2 + 3 O2 -> CO2 + 2 SO2
SO2는 유독가스!!!11
[해설작성자 : 김수야니] |
|
| 86. | 화학물질 취급 종사자가 200ppm의 아세톤에 3시간, 100ppm의 n-헥세인에 2시간 동안 노출되었을 때, 이 근로자의 8시간 기준 시간가중평균노출기준(TWA; ppm)은? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 69%
| | <문제 해설>
(200*3+100*2)/8=100
[해설작성자 : 웅냥냥] |
|
| 87. | 화재발생 후 화재의 진행단계에 따른 실험실 종사자의 적절한 대응으로 이루어진 것은? |

정답 : [4]☜ 블럭 설정하면 보임
정답률 : 81%
|
| 88. | 위험물안전관리법령상 질산에스테르류, 니트로화합물, 유기과산화물이 속하는 위험물 성질은? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 56%
|
| 89. | 산업안전보건법령상 자기반응성 물질 및 혼합물의 구분 형식 A~G 중 형식 A에 해당되는 것은? |
| 1. | 포장된 상태에서 폭굉하거나 급속히 폭연하는 자기반응성 물질 또는 화합물 |
| 2. | 50kg 포장물의 자기가속분해온도가 75℃보다 높은 물질 또는 혼합물 |
| 3. | 분해열이 300 J/g 미만인 물질 또는 혼합물 |
| 4. | 폭발성 물질 또는 화약류 물질 또는 혼합물 |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 60%
|
| 90. | GHS에 의한 화학물질의 분류에 있어 성상에 대한 설명으로 옳지 않은 것은? |
| 1. | 가스는 50℃에서 증기압이 300kPaAbs를 초과하는 단일 물질 또는 혼합물 |
| 2. | 고체는 액체 또는 가스의 정의에 부합되지 않는 단일 물질 또는 혼합물 |
| 3. | 증기는 액체 또는 고체 상태로부터 방출되는 가스 형태의 단일 물질 또는 혼합물 |
| 4. | 액체는 101.3 kPa에서 녹는점이나 초기 녹는점이 25℃ 이하인 단일 물질 또는 혼합물 |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 51%
| | <문제 해설>
4. 초기 녹는점이 "20'c" 이하인 단일 물질 또는 혼합물
[해설작성자 : KangCorn] |
|
| 91. | 산업안전보건법령상 물질안전보건자료의 경고표시 기재항목의 작성방법으로 틀린 것은? |
| 1. | 그림문자 : 5개 이상일 경우 4개만 표시 가능 |
| 2. | 신호어 : “위험” 또는 “경고” 표시 모두 해당하는 경우에는 “경고”만 표시가능 |
| 3. | 예방조치 문구 : 7개 이상인 경우에는 예방·대응·저장·폐끼 각 1개 이상을 포함하여 6개만 표시 가능 |
| 4. | 유해·위험 문구 : 해당 문구는 모두 기재하되, 중복되는 문구는 생략, 유사한 문구는 조합 가능 |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 75%
| | <문제 해설>
"위험" 만 표시가능~
[해설작성자 : 김수야니] |
|
| 92. | C2H4를 합성하기 위한 반응은 아래와 같으며, C2H4의 수득률이 42.5%라면 C2H4 281g을 생산하기 위해 필요한 C6H14의 질량(g)은? |
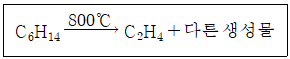
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 50%
| | <문제 해설>
C2H4 281g은 수득률 42.5%에 대한 값이므로 수득률이 100%일때는 약 661g 이다.
661g 나누기 1mol/28g(C2H4분자량)= 23.6mol
C6H14와 C2H4의 생성몰수와 반응몰수는 1:1로 동일하므로
C2H4 23.6mol의 생성을 위해서는 C6H14는 동일하게 23.6mol이 필요하다
C6H14 23.6mol * 86g/mol= 2.03*10^3
[해설작성자 : 김수야니] |
|
| 93. | 브뢴스테드에 의한 산/염기의 정의에 따라 아래 반응을 바르게 설명하지 못한 것은? |
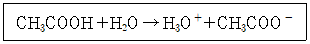 | 1. | 정반응에서 아세트산은 양성자를 잃으므로 산에 속한다. |
| 2. | 정반응에서 물은 양성자를 받아들임으로 염기에 속한다. |
| 3. | 역반응에서 하이드로늄 이온은 양성자를 잃으므로 산에 속한다. |
| 4. | 역반응에서 아세트산 이온은 양성자를 받아들임으로 산에 속한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 74%
| | <문제 해설>
H+줌 -> 산 <-> H+받음 -> 염기
역반응에서 CH3COO-는 H+ 받음-> 염기
[해설작성자 : 김수야니] |
|
| 94. | 화학 실험실 실험기구 및 장치의 안전 사용에 대한 설명으로 가장 거리가 먼 것은? |
| 1. | 모든 플라스크류는 감압조작에 사용할 수 있다. |
| 2. | 비커류에 용매를 넣을 때 크리프현상을 주의하여야 한다. |
| 3. | 실험 장치는 온도 변화에 따라 기계적 강도가 변할 수 있다. |
| 4. | 실험 장치는 사용하는 약품에 따라 기계적 강도가 변할 수 있다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 74%
| | <문제 해설>
감압 조작 시 압력에 의해 모양이 뒤틀리는 현상을 크리프 현상이라고 함.
삼각 플라스크는 감압 조작시 깨질 위험이 있으므로 사용할 수 없음.
[해설작성자 : KangCorn] |
|
| 95. | 비점이 다른 성분의 혼합물인 원유나 중질유 등의 유류저장탱크에 화재가 발생하여 장시간 진행되어 형성된 열류층이 탱크 저부로 내려오며 탱크 밖으로 비산, 분출되는 현상은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 67%
| | <문제 해설>
1. BLEVE: 고압 상태인 액화가스 용기가 가열되어 물리적 폭발이 화학적 폭발로 이어지는 현상
3. Flash-over : 실내에서 화재가 진행되며 불완전 연소로 인해 천장에 가연성 가스들이 축적되고 발화점에 다다랐을 때 폭발적인 연소가 진행되는 현상
4. Backdraft : 화재실의 문을 열면서 신선한 공기가 내부로 유입되어 실내에 축적되어 있던 가연성 가스가 단시간에 폭발적으로 연소함으로써 화재가 폭풍을 동반하며 실외로 분출되는 현상
[해설작성자 : KangCorn] |
|
| 96. | 위험물안전관리법령상 화학분석실에서 발생하는 위험 화학물질의 운반에 관한 설명으로 틀린 것은? |
| 1. | 위험물은 온도변화 등에 의하여 누설되지 않도록 하여 밀봉 수납한다. |
| 2. | 하나의 외장 용기에는 다른 종류의 위험물을 같이 수납하지 않는다. |
| 3. | 액체위험물은 운반용기 내용적의 98% 이하로 수납하되 55℃의 온도에서도 누설되지 않도록 충분한 공간용적을 유지해야 한다. |
| 4. | 고체위험물은 운반용기 내용적의 98% 이하로 수납해야 한다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 64%
| | <문제 해설>
[별표 19] [개정 2017. 7. 26.]
위험물의 운반에 관한 기준(제50조관련)
Ⅰ. 운반용기
(-중간 생략-)
다. 고체위험물은 운반용기 내용적의 95% 이하의 수납율로 수납할 것
라. 액체위험물은 운반용기 내용적의 98% 이하의 수납율로 수납하되, 55도의 온도에서 누설되지 아니하도록 충분한 공간용적을 유지하도록 할 것
[해설작성자 : 밀양금성컴퓨터학원 ☎055-354-3344] |
|
| 97. | 위험물안전관리법령상 ( )에 해당하는 용어는? |

정답 : [3]☜ 블럭 설정하면 보임
정답률 : 75%
|
| 1. | 완충용액이란 외부에서 어느 정도의 산이나 염기를 가했을 때, 영향을 크게 받지 않고 수소이온 농도를 일정하게 유지하는 용액이다. |
| 2. | 약염기에 그 염을 혼합시킨 완충용액은 강염기를 소량 첨가하면 pH의 변화가 크다. |
| 3. | 약산에 그 염을 혼합시킨 완충용액은 강산을 소량 첨가해도 pH의 변화가 그다지 없다. |
| 4. | 완충용액은 피검액의 안정제나 pH 측정의 비교 표준액으로 사용된다. |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 67%
| | <문제 해설>
pH 변화 크지 않다.
[해설작성자 : 만거] |
|
| 99. | 위험물안전관리법령상 인화성고체로 분류하는 1기압에서의 인화점 기준은? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 60%
|
| 100. | 소방시설법령상 특급 소방안전관리대상물의 소방안전관리자로 선임할 수 있는 자격기준으로 옳지 않은 것은? |
| 1. | 소방기술사 또는 소방시설관리사의 자격이 있는 사람 |
| 2. | 소방설비기사의 자격을 취득한 후 5년 이상 1급 소방안전관리대상물의 소방안전관리자로 근무한 실무경력이 있는 사람 |
| 3. | 소방설비산업기사의 자격을 취득한 후 6년 이상 1급 소방안전관리대상물의 소방안전관리자로 근무한 실무경력이 있는 사람 |
| 4. | 소방공무원으로 20년 이상 근무한 경력이 있는 사람 |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 59%
|
화학분석기사 필기 기출문제(해설) 및 CBT 2021년09월12일을 이용해 주셔서 감사합니다.
, 필기, 기출문제, 전자문제집, CBT, 온라인, 모의테스트, 모의고사


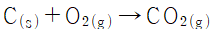

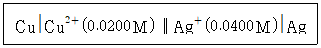

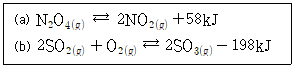
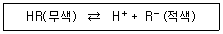




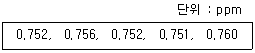





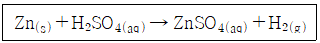

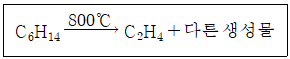
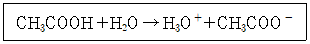

 광학기사 필기 기출문제(해설) 및 전자문제집 CBT 2008년07월27일...
광학기사 필기 기출문제(해설) 및 전자문제집 CBT 2008년07월27일...