위 이미지를 클릭하시면 인터넷으로 바로 문제를 풀어 보실수 있습니다.
(해설, 모의고사, 오답노트, 워드, 컴활, 정보처리 상설검정 프로그램 기능 포함)
전자문제집 CBT란?
종이 문제집이 아닌 인터넷으로 문제를 풀고 자동으로 채점하며 모의고사, 오답 노트, 해설까지 제공하는
무료 기출문제 학습 프로그램으로 실제 상설검정에서 사용하는 OMR 형식의 CBT를 제공합니다.
최신 9급 지방직 공무원 서울시 화학 필기 기출문제(해설) : [다운로드]
9급 지방직 공무원 서울시 화학 필기 기출문제(해설) 및 전자문제집 CBT 2019년 06월 15일(4092777)| 1. |  의 양성자, 중성자, 전자 수가 바르게 적힌 것은? 의 양성자, 중성자, 전자 수가 바르게 적힌 것은? |
| 1. | 양성자: 9, 중성자: 10, 전자: 9 |
| 2. | 양성자: 10, 중성자: 9, 전자: 9 |
| 3. | 양성자: 10, 중성자: 9, 전자: 10 |
| 4. | 양성자: 9, 중성자: 10, 전자: 10 |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 62%
| | <문제 해설>
양성자 9, 중성자 10, 전자 9에서 전자 하나 추가로 전자는 10
[해설작성자 : CEX] |
|
| 2. | <보기>는 수소와 질소가 반응하여 암모니아를 만드는 화학 반응식이다. 이에 대한 설명으로 가장 옳은 것은? (단, 수소 원자량은 1.0g/mol, 질소 원자량은 14.0g/mol 이다.) |
 | 1. | 암모니아를 구성하는 수소와 질소의 질량비는 3 : 14이다. |
| 2. | 암모니아의 몰질량은 34.0g/mol이다. |
| 3. | 화학 반응에 참여하는 수소 기체와 질소 기체의 질량비는 3 : 1이다. |
| 4. | 2몰의 수소 기체와 1몰의 질소 기체가 반응할 경우 이론적으로 2몰의 암모니아 기체가 생성된다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 66%
| | <문제 해설>
1. N:14g/mol H3:3g/mol따라서 비는 3:14
2. NH3의 분자량은 17g/mol
3. 화학식의 몰비는 3:1이고 질량비는 3:14
4. 화학식의 몰비는 3:1:2
[해설작성자 : ㅁㅇㄹ] |
|
| 3. | 물에 1몰이 녹았을 때 1몰의 A2+와 2몰의 B- 이온으로 완전히 해리되는 미지의 고체 시료 AB2를 생각해 보자. AB2 15g을 물 250g에 녹였을 때 물의 끓는점이 1.53K 증가함이 관찰되었다. AB2의 몰질량[g/mol]은 얼마인가? (단, 물의 끓는점 오름 상수(Kb)는 0.51K· kg· mol-1로 한다.) |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 60%
|
| 4. | -b[W]/dt=k[W]2로 반응속도가 표현되는 화학종 W를 포함하는 화학 반응에 대하여, 가장 반감기를 짧게 만들 수 있는 방법으로 옳은 것은? |
| 4. | 속도상수 k와 W의 초기 농도를 각각 3배로 크게 한다. |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 58%
|
| 5. | 암모니아의 합성 반응이 <보기>에 제시되었으며, 특정 실험 온도에서 K값이 6.0×10-2으로 알려져 있다. 해당 온도에서 초기 농도가 [N2]=1.0M, [H2]=1.0×10-2M, [NH3]=1.0×10-4M일 때, 평형에 도달하기 위해 화학 반응이 이동하는 방향을 예측한다면? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 71%
|
| 6. | 25℃에서 어떤 수용액의 [H+]=2.0×10-5M일 때, 이 용액의 [OH-] 값[M]으로 옳은 것은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 58%
|
| 7. | 외벽이 완전히 단열된 6kg의 철 용기에 담긴 물 23kg이 20℃의 온도에서 평형상태에 존재한다. 이 물에 온도가 70℃인 10kg의 철 덩어리를 넣고 평형에 도달하게 하였을 때 물의 최종 온도[℃]는? (단, 팽창 또는 수축에 의한 영향은 무시한다. 모든 비열은 온도에 무관하다고 가정하며, 물의 비열은 4kJ · kg-1·℃sup>-1, 철의 비열은 0.5kJ · kgsup>-1·℃sup>-1로 한다.) |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 56%
|
| 8. | KOH(aq)와 Fe(NO3)2(aq)의 균형이 맞추어진 화학 반응식에서 반응물과 생성물의 모든 계수의 합은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 56%
|
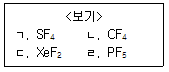
| 9. | <보기>의 물질 중 입체수(SN, steric number)가 다른 물질은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 56%
| | <문제 해설>
ㄱ,ㄷ,ㄹ 총 5개의 입자수
ㄴ은 총 4개의 입자수
중간의 원소와 결합된 수+ 비공유전자쌍= 입체수
[해설작성자 : 난 화학 망한거 같아...] |
|
| 10. | <보기>에 제시된 이상 기체 및 실제 기체에 대한 방정식을 설명한 것으로 가장 옳지 않은 것은? |
 | 1. | 실제 기체 입자들 사이에서 작용하는 인력을 고려할 때, 일정한 압력에서 온도가 낮을수록 실제 기체는 이상 기체에 가까워진다. |
| 2. | 실제 기체 입자들 사이에서 작용하는 인력을 보정하기 위해 P대신 [P+a(n/V)2]를 사용한다. |
| 3. | 실제 기체는 기체 입자가 부피를 가지고 있으므로 이를 보정하기 위해 V대신 V-nb를 사용한다. |
| 4. | 실제 기체는 낮은 압력일수록 이상 기체에 근접한다. |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 59%
|
| 11. | 완충 용액에 대한 설명 중 가장 옳지 않은 것은? |
| 1. | 완충 용액은 약산과 그 짝염기의 혼합으로 만들 수 있다. |
| 2. | 완충 용액은 약염기와 그 짝산의 혼합으로 만들 수 있다. |
| 3. | 완충 용액은 센산(strong acid)이나 센염기(strong base)가 조금 가해졌을 때 pH가 잘 변하지 않는다. |
| 4. | 완충 용량은 pH가 완충 용액에서 사용하는 약산의 pKa에 근접할수록 작아진다. |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 64%
|
| 12. | 약산인 아질산(HNO2)은 0.23M의 초기 농도를 갖는 수용액일 때 2.0의 pH를 갖는다. 아질산의 산 이온화 상수(acid ionization constant)인 Ka는? |
정답 : [3]☜ 블럭 설정하면 보임
정답률 : 54%
|
| 13. | PCl3 분자의 VSEPR 구조와 PCl3 분자에서 P 원자의 형식 전하를 옳게 짝지은 것은? |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 52%
|
| 14. | 다음 중에서 가장 작은 이온 반지름을 가지는 이온은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 65%
|
| 15. | 탄소(C(s)), 수소(H2(g)), 메테인(CH4(g))의 연소 반응 (생성물은 기체 이산화탄소와 액체 물 또는 두 물질 중 하나임.)은 각각 순서대로 390kJ/mol, 290kJ/mol, 890kJ/mol의 열을 방출하는 반응이다. <보기> 반응에서 방출하는 열[kJ/mol]은? |

정답 : [1]☜ 블럭 설정하면 보임
정답률 : 48%
|
| 16. | 어떤 동핵 이원자 분자(X2)의 전자 배치는 <보기>와 같다. 이 분자의 결합 차수는 얼마인가 ? |

정답 : [1]☜ 블럭 설정하면 보임
정답률 : 59%
|
| 17. | 미지의 화학종 A가 포함된 두 가지 반쪽반응의 표준환원전위(E°)는 각각 E°(A2+|A)=+0.3V와 E°(A+|A)=+0.4V이다. 이를 바탕으로 계산한 E°(A2+|A+) 값[V]은? |
정답 : [1]☜ 블럭 설정하면 보임
정답률 : 23%
|
| 18. | S2- 이온의 전자 배치를 옳게 나타낸 것은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 65%
|
| 19. | HSO4-(Ka=1.2×10-2), HNO2(Ka=4.0×10-4), HOCl(Ka=3.5×10-8), NH4+(Ka=5.6×10-10) 중 1M의 수용액을 형성하였을 때 가장 높은 pH를 보이는 일양성자산은? |
정답 : [2]☜ 블럭 설정하면 보임
정답률 : 46%
|
| 20. | 강산인 0.10M HNO3용액 0.5L에 강염기인 0.12M KOH용액 0.5L를 첨가하였다. 반응이 완료된 후의 pH는? (단, 생성물로 생기는 물의 부피는 무시한다.) |
정답 : [4]☜ 블럭 설정하면 보임
정답률 : 53%
|
9급 지방직 공무원 서울시 화학 필기 기출문제(해설) 및 CBT 2019년 06월 15일(4092777)을 이용해 주셔서 감사합니다.

 의 양성자, 중성자, 전자 수가 바르게 적힌 것은?
의 양성자, 중성자, 전자 수가 바르게 적힌 것은?



